فهرست مطالب
یونها در آب: تبادل یون چیست، یون ها چگونه عمل میکنند و چرا مهم هستند
یونها ذراتی با بار الکتریکی هستند (اتمها یا مولکولها) که در آب حل میشوند و به آن خاصیت یونی میدهند. این یونها نقش مهمی در شیمی آب و فرآیندهای تصفیه آن ایفا میکنند.
دو نوع اصلی یون در آب وجود دارد:
-
کاتیونها (Cations): یونهای با بار مثبت (مانند ⁺Na⁺، Ca²)
-
آنیونها (Anions): یونهای با بار منفی (مانند ⁻Cl⁻، SO₄²)
آب به طور کلی از نظر الکتریکی خنثی است؛ یعنی تعداد بارهای مثبت و منفی آن برابر است. در غیر این صورت، تماس دست با آب باعث شوک الکتریکی میشد!
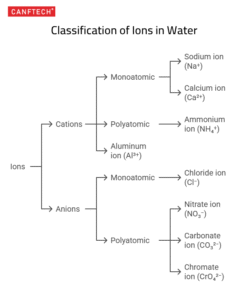
انواع یونها
یونها میتوانند دارای بار الکتریکی ۱+ تا ۳+ یا ۱- تا ۳- باشند. از نظر ساختار نیز در دو دسته قرار میگیرند:
-
یونهای تکاتمی (Monoatomic): از یک اتم تشکیل شدهاند.
-
یونهای چنداتمی (Polyatomic): از چند اتم به هم پیوسته ساخته شدهاند که در کل یک ذره باردار محسوب میشوند.
مثالهایی از یونهای رایج در آب
| نوع یون | مثال و فرمول |
|---|---|
| کاتیون تکظرفیتی تکاتمی | یون سدیم (⁺Na) |
| کاتیون دوظرفیتی تکاتمی | یون کلسیم (⁺Ca²) |
| کاتیون تکظرفیتی چنداتمی | یون آمونیوم (⁺NH₄) |
| آنیون تکظرفیتی تکاتمی | یون کلرید (⁻Cl) |
| آنیون تکظرفیتی چنداتمی | یون نیترات (⁻NO₃) |
| آنیون دوظرفیتی چنداتمی | یون کربنات (⁻CO₃²) |
| آنیون دوظرفیتی چنداتمی (فلزی) | یون کرومات (⁻CrO₄²) |
| کاتیون سهظرفیتی تکاتمی (در محیط اسیدی) | یون آلومینیوم (⁺Al³) |
نکته: در آب معمولی، آنیونهای تکاتمی دوظرفیتی یا سهظرفیتی وجود ندارند.
رفتار یونها در آب
یونها در آب آزادانه حرکت میکنند و به صورت جفتهای ثابت باقی نمیمانند. تعادل بار مثبت و منفی در آب همیشه حفظ میشود.
حل شدن نمکها
نمکها ترکیبات بلوری هستند که نسبت مشخصی از کاتیونها و آنیونها دارند.
برای مثال:
-
نمک طعام (NaCl): در آب حل شده و به یونهای ⁺Na و ⁻Cl تفکیک میشود.
یونهای حل شده توسط مولکولهای آب احاطه میشوند (پدیده آبدار شدن یا Hydration):
-
کاتیونها به سمت اکسیژن مولکولهای آب جذب میشوند.
-
آنیونها به سمت هیدروژن مولکولهای آب جذب میشوند.
مثالهایی از نمکهای حل شده در آب
-
سولفات منیزیم (MgSO₄): یونهای ⁺Mg² و ⁻SO₄²
-
کلرید کلسیم (CaCl₂): هر یون ⁺Ca² با دو یون ⁻Cl متعادل میشود.
-
کربنات سدیم (Na₂CO₃): هر یون ⁻CO₃² با دو یون ⁺Na متعادل میشود.
مواد جامد محلول کل (TDS)
زمانی که آب تبخیر میشود، باقیمانده جامدات محلول بهجا میماند که شامل نمکها، سیلیس و ترکیبات آلی است:
-
آب دریا: TDS بالا (۳۵–۴۰ گرم در لیتر)
-
آب رودخانه/آب لولهکشی: TDS پایینتر (۵۰–۵۰۰ میلیگرم در لیتر)
TDS شاخص مهمی در ارزیابی کیفیت آب محسوب میشود.
تبادل یونی و جرم معادل: چگونه تبادل یونی با محاسبه دقیق یونها انجام میشود؟
در فرآیند تصفیه آب با تبادل یونی، حذف یونهای محلول از آب با دقت بالایی انجام میشود. اما یک نکته کلیدی در طراحی سیستمهای تبادل یونی این است که بدانیم چند یون و با چه مقدار رزین باید مبادله شوند. برای این منظور، از مفهوم مهمی به نام جرم معادل (Equivalent Mass) استفاده میشود.
جرم معادل در تبادل یونی چیست؟
جرم معادل نشاندهنده مقدار یون موردنظر (بر حسب گرم) است که میتواند یک بار الکتریکی (یک واحد ظرفیت تبادل) را در فرآیند تبادل یونی تأمین کند.
به عبارت سادهتر، برای اینکه بدانیم چند گرم از یک یون را باید با رزین تبادل کنیم، باید جرم معادل آن را محاسبه کنیم.
فرمول محاسبه جرم معادل
۱ مولاریته * ظرفیت یونی (Valence) = اکی والان بر لیتر (eq/L)
- ظرفیت یونی (Valence): تعداد بارهای الکتریکی یون (۱+، ۲+، ۳+، ۱-، ۲-و …)
- به ازای هر بار یونی، مقدار مشخصی از رزین موردنیاز است.
مثالهای جرم معادل برای یونهای رایج
| یون | مولاریته (mol/L) | ظرفیت یونی | اکی والان بر لیتر (eq/L) |
|---|---|---|---|
| Na⁺ (سدیم) | ۲۳.۰۰ | ۱+ | ۲۳.۰۰ |
| Ni²⁺ (نیکل) | ۵۸.۷۰ | ۲+ | ۲۹.۳۵ |
| Ca²⁺ (کلسیم) | ۴۰.۰۸ | ۲+ | ۲۰.۰۴ |
| SO₄²⁻ (سولفات) | ۹۶.۰۶ | ۲- | ۴۸.۰۳ |
چرا مولاریته در طراحی سیستمهای تبادل یونی مهم است؟
✅ به کمک مولاریته میتوان:
- مقدار رزین تبادل یونی مناسب برای حذف یونهای محلول را دقیقاً محاسبه کرد.
- مقدار محلول احیاکننده (Regenerant) موردنیاز را تعیین کرد.
- راندمان و طول عمر ستونهای تبادل یونی را بهینه کرد.
- میزان ظرفیت واقعی رزینها را در شرایط مختلف کاری پیشبینی کرد.
کاربرد مولاریته در تصفیه آب صنعتی
در کاربردهای پیشرفته مانند:
- تصفیه آب نیروگاهها
- حذف سختی آب (Water Softening)
- دیونیزهکردن آب برای صنایع دارویی و الکترونیک
- تصفیه آب شرب
محاسبه صحیح مولاریته کلید دستیابی به عملکرد بهینه سیستم تبادل یونی است.
تبادل یونی: حذف ناخالصیها از آب
ناخالصیهای موجود در آب
آب به طور طبیعی حاوی مقدار کمی مواد خارجی است. بسیاری از این مواد بیخطر بوده و حتی برای سلامتی مفید هستند (آب آشامیدنی با میزان مناسب املاح معدنی برای بدن بهتر است از آب کاملاً خالص).
اما در برخی کاربردهای خاص — مانند صنایع دارویی، تولید نیمههادیها یا نیروگاهها — همین مقدار کم مواد حل شده نیز ناخالصی محسوب میشود و باید حذف گردد.
انواع ناخالصیهای آب
-
مواد نامحلول (شن، رسوبات، ذرات آلی):
با فیلتراسیون قابل حذف هستند.
امروزه انواع فیلترها از فیلترهای ساده تا اولترافیلتراسیون (برای حذف ذرات بسیار ریز) در دسترس است. -
مواد محلول:
-
مواد غیر یونی: توسط کربن فعال یا اسمز معکوس حذف میشوند.
-
مواد یونی (یونها): بهترین روش برای حذف آنها تبادل یونی است.
-
تبادل یونی چیست؟
تبادل یونی فرآیندی است که در آن یونهای نامطلوب موجود در آب با یونهای مطلوبتر تعویض میشوند. این کار به کمک رزینهای تبادل یونی انجام میشود.
کاربردهای رایج تبادل یونی:
-
نرم کردن آب (Water Softening)
-
دیونیزه کردن آب (Demineralization)
-
حذف انتخابی یونهای خاص
-
تصفیه آب صنعتی
رزینهای تبادل یونی: نحوه عملکرد
رزینهای تبادل یونی ذرات پلاستیکی بسیار ریز و متخلخل هستند (قطر حدود ۰.۶ میلیمتر). هر دانه رزین:
-
از پلیمر مقاوم ساخته شده است.
-
دارای گروههای باردار ثابت است که به ساختار آن متصل شدهاند.
-
یونهای متحرک (Counterions) را در خود نگه میدارد که میتوانند در داخل و خارج از دانه رزین حرکت کنند.
رزینها همچنین درون ساختار متخلخل خود آب ذخیره میکنند (به این مقدار، رطوبت رزین گفته میشود).
حفظ تعادل الکتریکی
برای حفظ تعادل الکتریکی، هر یون وارد شده به دانه رزین باید باعث خروج یون همبار شود:
-
فقط یونهایی با بار الکتریکی یکسان میتوانند با هم تعویض شوند (کاتیون ↔ کاتیون، آنیون ↔ آنیون).
انواع رزینهای تبادل یونی
رزین تبادل کاتیونی
-
گروه باردار: سولفونات (⁻SO₃)
-
یون متحرک رایج: سدیم (⁺Na)
-
مثال: TC008 Canftech
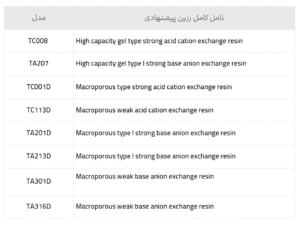
رزین تبادل آنیونی
-
گروه باردار: آمونیوم چهارتایی (CH₂—N⁺(CH₃)₃)
-
یونهای متحرک: ⁻Cl⁻، OH و غیره.
نکته مهم:
نمیتوان از یک رزین برای تعویض همزمان کاتیونها و آنیونها استفاده کرد؛ زیرا بارهای مثبت و منفی ثابت داخل رزین یکدیگر را خنثی میکنند و امکان تبادل یونی از بین میرود. به همین دلیل در سامانههای تبادل یونی، به صورت جداگانه از رزینهای کاتیونی و رزینهای آنیونی استفاده میشود.
فرآیند تبادل یونی در چه صنایعی کاربرد دارد؟
-
- صنایع غذایی و نوشیدنی
- صنایع شیمیایی و پتروشیمیایی
- صنایع دارویی
- قند و شکر
- نیروگاه های هستهای
- نیمه رساناها
- تصفیه آبهای زیرمینی
- تصفیه فاضلاب
- تولید آب شرب
- صنایع هستهای و الکترونیکی
جمعبندی اصول تبادل یونی
| نوع رزین | تبادل میکند | گروه ثابت نمونه | یون متحرک نمونه |
|---|---|---|---|
| رزین تبادل کاتیونی | کاتیونها | سولفونات (⁻SO₃) | ⁺Na⁺، Ca²⁺، Mg² |
| رزین تبادل آنیونی | آنیونها | آمونیوم چهارتایی (N⁺R₃) | ⁻Cl⁻، SO₄²⁻،NO₃ |

